Anvisa aprova primeiro autoteste para Covid-19 no Brasil
Disponibilidade no mercado depende da empresa detentora do registro

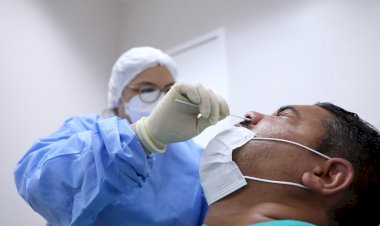
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, nesta quinta-feira (17), o primeiro autoteste para Covid-19 no país.
O produto registrado pela Anvisa é o Novel Coronavírus (Covid-19) Autoteste Antígeno, da empresa CPMH Comércio e Indústria de Produtos Médicos-Hospitalares e Odontológicos.
Agora, a disponibilidade no mercado depende da empresa detentora do registro.
O produto funciona com swab nasal não profundo e apresenta resultados em 15 minutos.
“Para conceder o registro a Anvisa analisa uma série de requisitos técnicos, entre os quais estão a usabilidade e o gerenciamento de risco, que servem para adequar o produto para uso por pessoas leigas dando maior segurança no seu uso”, diz a agência em comunicado.
A avaliação do pedido de registro na Anvisa levou 16 dias, incluindo quatro utilizados pela empresa solicitante para atender exigências técnicas feitas pela Anvisa.
A publicação do registro foi ontem no Diário Oficial da União.
Outros pedidos
A Anvisa autorizou o uso de autotestes de Covid-19 no Brasil há 20 dias, no último dia 28 de janeiro. Com a aprovação, fica permitida a venda dos exames por farmácias e estabelecimentos de saúde licenciados para comercializar dispositivos médicos.
No entanto, a comercialização, distirbuição e o uso no país dependem de a Anvisa autorizar empresas produtoras dos autotestes.
Além da Novel, outras 67 empresas fizeram pedidos de registros de autotestes à Anvisa. Desses, dez tiveram o registro reprovado e outras duas estão “em análise do cumprimento de exigência”, uma das últimas etapas antes de possível aprovação.
Requisitos para o registro
Entre os requisitos para conceder o registro, a Anvisa determina que os produtos devem apresentar instruções de uso, armazenagem e descarte. As informações precisam contar com uma linguagem simples e com ilustrações, para facilitar o manuseio e a interpretação do resultado.
Com relação à embalagem, as orientações da Anvisa informam que o rótulo externo do produto deve conter todos os componentes do kit que são necessários para a realização do teste, além da validade do dispositivo.
Além disso, o fabricante deve oferecer um canal de atendimento ao usuário para orientar e encaminhar as demandas sobre o uso do produto e como proceder após a obtenção do resultado.
Segundo a Anvisa, além de disponibilizar o contato desse serviço de atendimento, a empresa deve indicar o serviço Disque Saúde do Ministério da Saúde, de acordo com as recomendações do Plano Nacional de Expansão da Testagem para Covid-19, o PNE-Teste.
Por: Kaluan BernardoLucas Rocha