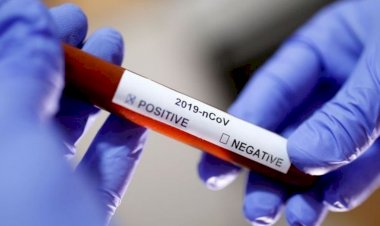
Anvisa autoriza por unanimidade o uso de autotestes de Covid-19 no Brasil
Decisão foi divulgada nesta sexta-feira (28), após votação da Diretoria Colegiada da agência a partir de análise de informações complementares enviadas pelo Ministério da Saúde
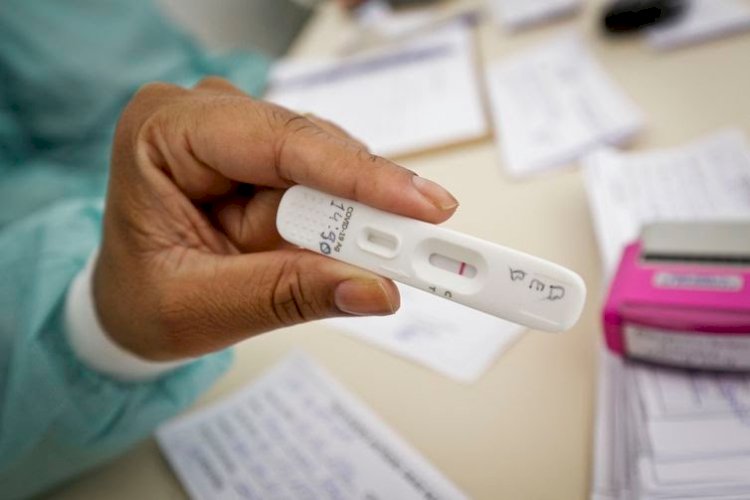
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou o uso de autotestes de Covid-19 no Brasil. A decisão aconteceu nessa sexta-feira (28), após votação da Diretoria Colegiada da agência a partir da análise da solicitação e envio de informações complementares pelo Ministério da Saúde.
Autorização permite a comercialização dos testes em farmácias e estabelecimentos de saúde. Os exames, que podem ser feitos em casa, permitem realizar o acompanhamento das condições da doença. No entanto, os testes não são conclusivos para o diagnóstico segundo a Anvisa.
Na abertura da reunião, transmitida ao vivo pelas redes sociais da Anvisa, a diretora Meiruze Sousa Freitas destacou que o diretor-presidente Antônio Barra Torres não participou do evento por questões de saúde na família.
Votaram a favor os diretores Meiruze Sousa Freitas, Cristiane Rose, Romison Rodrigues Mota e Alex Machado Campos. A decisão, que acontece por maioria simples dos votos, foi tomada por unanimidade.
Destaques da votação
Durante a votação, os diretores destacaram os aspectos principais que levaram à autorização pela agência.
A diretora Cristiane Rose Jourdan destacou o contexto do aumento significativo de casos da doença no país devido ao avanço da variante Ômicron do novo coronavírus, altamente contagiosa.
"O produto de diagnóstico in vitro na forma de autoteste pode representar excelente estratégia de triagem e medida adicional no controle da pandemia, principalmente nesse momento em que o contágio pela doença é grande e muitas pessoas não conseguem ter acesso aos testes pelo SUS ou por laboratórios na rede privada”, disse Cristiane.
O diretor Rômison Rodrigues Mota destacou que os autotestes podem contribuir para reduzir a disseminação do novo coronavírus.
“Ao possibilitar o registro de dispositivos médicos para diagnóstico in vitro para detecção do antígeno do SARS-CoV-2 como autoteste cumpre a finalidade institucional desta Anvisa, uma vez que abre possibilidade de ampliar o acesso da sociedade a testes que permitam a rápida detecção do vírus”, disse.
A opinião foi compartilhada pelo diretor Alex Machado Campos. “O papel dos autotestes nesse momento, com a participação e o envolvimento direto do cidadão pode contribuir, não há dúvida, significativamente para que nós possamos quebrar cadeias de transmissão”, afirmou.
A diretora Meiruze Sousa Freitas ressaltou que, para que os testes sejam comercializados, as empresas devem realizar o pedido de registro junto à Anvisa. A liberação acontecerá após a avaliação da agência de características como segurança e precisão dos exames.
“Com a aprovação dessa regulamentação, não significa que o autoteste vai estar disponível hoje ou amanhã em um estabelecimento autorizado à sua comercialização. É preciso que uma empresa regularizada venha à Anvisa e registre o seu autoteste”, disse Meiruze.
Fonte: CNN Brasil