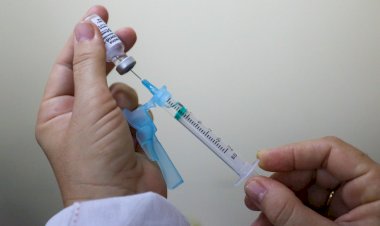
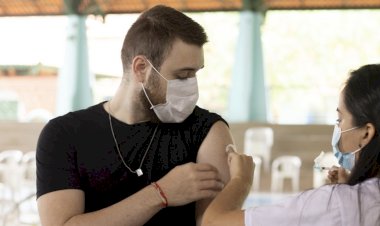
Atualização de vacina bivalente contra Covid é eficaz e segue rigor científico; entenda
Em vídeo que circula nas redes sociais, um médico põe em dúvida a eficácia da nova versão da Pfizer, após EUA aprovarem o imunizante com estudos pré-clínicos. Mas essas pesquisas são suficientes para garantir a segurança por se tratar da atualização de uma vacina comprovadamente eficaz.
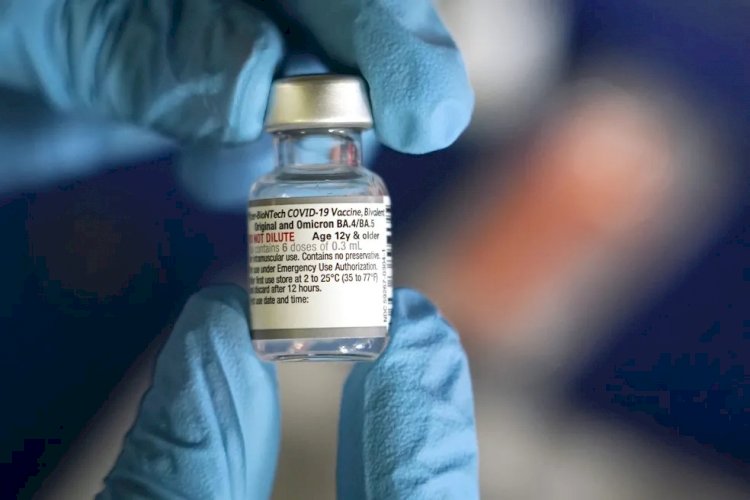
Circula nas redes sociais o vídeo de um médico citando que a vacina bivalente BA.4/BA.5 da Pfizer contra a Covid-19 não passou por testes clínicos (com humanos) antes de ser aprovada pela agência reguladora de medicamentos dos Estados Unidos (FDA, na sigla em inglês).
No vídeo, publicado em setembro do ano passado e que ganhou visibilidade recentemente, o médico Roberto Zeballos também cita que quem pegou Covid está mais do que protegido, o que não é verdade (estudos já comprovaram os riscos da infecção). Considerado por seus pares como um médico antivacina, a postura de Zeballos na pandemia já foi alvo de nota de repúdio de professores de medicina da Unifesp (Universidade Federal de São Paulo) ainda em 2022.
O infectologista Renato Kfouri, vice-presidente da Sociedade Brasileira de Imunizações (SBIm), aponta que as afirmações do médico sobre a vacina bivalente induzem a erro e não retratam o rigor científico com que o imunizante foi analisado e aprovado.
O reforço bivalente da Pfizer foi liberado nos EUA em agosto de 2022. A FDA - órgão equivalente à Anvisa nos EUA - usou três fontes de dados para analisar o novo imunizante: dados da vacina monovalente (primeira versão do imunizante), de um estudo clínico (com humanos) da bivalente BA.1 e de estudos pré-clínicos da versão BA.4/BA.5.
Vale reforçar a diferença entre duas fases comuns nos estudos de uma vacina:
- ???? Estudos pré-clínicos são feitos em animais ou in vitro para avaliar a toxicidade e os efeitos gerais do candidato a medicamentos.
- ???? Estudos clínicos envolvem o teste em humanos, em grupos selecionados e com pessoas que recebem o imunizante tendo seus resultados comparados com pessoas que não receberam.
Aprovação de atualização sem testes em humanos é normal
A aprovação da FDA segue um protocolo normal no meio científico e não pode ser base para afirmações contra a vacina, como explicou o infectologista Renato Kfouri, vice-presidente da Sociedade Brasileira de Imunizações (SBIm).