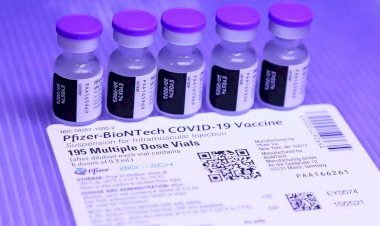
CoronaVac para crianças de 3 a 5 anos é aprovada pela Anvisa; decisão foi unânime
Vacina já estava liberada para crianças a partir de 6 anos.
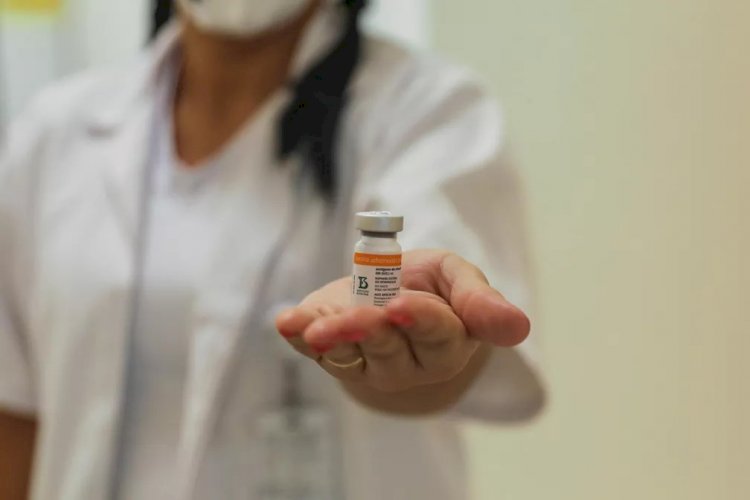
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou nesta quarta-feira (13) a autorização da aplicação da vacina CoronaVac em crianças de 3 a 5 anos.
A decisão foi unânime: todos os diretores da agência deram voto favorável à autorização da aplicação.
Veja, abaixo, cinco pontos de destaque da aprovação:
- CoronaVac está liberada para crianças a partir de 3 anos
- Poderá ser aplicada em imunossuprimidos, que são pessoas com baixa imunidade
- Imunização será em duas doses aplicadas em intervalo de 28 dias
- Vacina é a mesma usada em adultos, sem adaptação de versão pediátrica
- Anvisa não determinou quando começa a vacinação: distribuição de doses, cronograma e alteração de planos dependem dos estados e do Ministério da Saúde.
A decisão foi tomada após a análise de um pedido apresentado pelo Instituto Butantan em 11 de março para liberação do imunizante contra a Covid-19 para essa faixa etária.
(Correção: o g1 errou ao afirmar que a CoronaVac não foi aprovada para imunossuprimidos. A aplicação neste público também foi autorizada. O erro foi corrigido às 19h10 desta quarta, 13.)
A Coronavac está autorizada para uso emergencial no Brasil desde o dia 17 de janeiro de 2021, mas foi somente em janeiro de 2022 que a agência regulatória autorizou a ampliação do uso da vacina para crianças e adolescentes de 6 a 17 anos de idade.
Os cinco diretores que votaram com a relatora Meiruze Freitas aprovaram a aplicação também para o grupo de imunossuprimidos, pessoas que têm baixa imunidade.
"Apesar de as crianças não serem o rosto da pandemia, elas podem estar entre as maiores vítimas" disse Meiruze Freitas, segunda diretora da Anvisa e relatora do processo de aprovação.
"Sabemos que todas as crianças de diversos países estão sendo afetadas, mas os efeitos nocivos serão maiores para as mais vulneráveis, tanto economicamente, quanto para as com saúde mais debilitadas", acrescentou
Aplicação depende do Ministério da Saúde
A aprovação da Anvisa para essa faixa etária segue agora para a Câmara Técnica de Assessoramento em Imunização da Covid-19 do Ministério da Saúde.
Renato Kfouri, pediatra infectologista e diretor da Sociedade Brasileira de Imunização, explica que a aprovação depende dessa análise técnica do governo federal para que a imunização desse público seja de fato iniciada.
"[Além disso], precisamos ver quantas doses temos nos estados e municípios, quantas o Butantan consegue fabricar e em que espaço de tempo, nós vamos precisar no entorno de 10 milhões de doses para incluir essa população de 3 a 5 anos", ressalta o médico.
O g1 entrou em contato com o Ministério da Saúde questionando quantas doses serão distribuídas e qual o cronograma da pasta, mas o Ministério respondeu apenas que "vai avaliar, junto à Câmara Técnica Assessora em Imunizações, o uso do imunizante nesta faixa etária".
Nesta quarta, logo após aprovação da Anvisa, o Instituto Butantan anunciou que pediu que a CoronaVac seja incluída no Programa Nacional de Imunizações para crianças de 3 a 5 anos.
Em nota, o Butantan declarou que "espera agora que o imunizante seja incorporado ao Programa Nacional de Imunizações (PNI) do Ministério da Saúde, de acordo com a demanda necessária e mediante contratação".
Esquema vacinal e composição
O esquema vacinal para crianças a partir de 3 anos é o mesmo recomendado para os adultos: duas doses aplicadas em um intervalo de 28 dias. A vacina será a mesma já aplicada na população em geral.
A mudança na faixa etária foi defendida na análise de Gustavo Mendes, gerente de medicamentos da Anvisa.
"Nós temos uma realidade em que o contexto exige ações, estratégias para que a gente possa garantir uma cobertura vacinal, mas é preciso acompanhamento dos compromissos e dados para que a gente possa saber por quanto tempo estamos protegidos, quando vamos precisar de doses de reforço, como é o esquema vacinal para o futuro e o desempenho frente às variantes", disse o gerente de medicamentos.
Especialistas e entidades defenderam a ampliação
Durante a reunião, a Anvisa também apresentou considerações de especialistas e entidades médicas para a aprovação da vacina para crianças a partir de 3 anos.
Para a Sociedade Brasileira de Imunizações, Sociedade Brasileira de Infectologia, Sociedade Brasileira de Pneumologia e Tisiologia, os benefícios da imunização nessa faixa etária superam os eventuais riscos associados à vacinação.
Apesar disso, as entidades sugeriram a realização de estudos que possam identificar a possibilidade de coadministração com outras vacinas pediátricas e uso da vacina em esquemas alternativos, com doses de reforço e intervalos de doses superiores.
"A doença é menos grave nas crianças, mas não significa que não traga risco de hospitalização e morte", avaliou também Marco Aurélio Sáfadi, infectologia e presidente do Departamento de Infectologia da Sociedade Brasileira de Pediatria.
Durante a apresentação do seu parecer, o especialista defendeu que estender a vacinação para esse grupo é uma estratégia importante para diminuir carga de hospitalizações e mortes dessas crianças.
"Até o momento no país já registramos mais de 12 mil hospitalizações e 952 mortes atribuídas a Covid19 nessa faixa etária", relembrou.
Vacinação em crianças
Dados do consórcio de veículos de imprensa apontam que 13.094.879 doses foram aplicadas em crianças de 5 a 11 anos, que estão parcialmente imunizadas - o número representa quase 63,88% da população nessa faixa etária que tomou a primeira dose.
Ainda nesta faixa, 8.111.105 estão totalmente imunizadas ao tomar a segunda dose de vacinas, o que corresponde a 39,57% da população deste grupo.
Fonte: G1